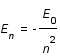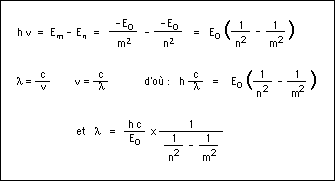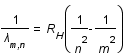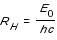Presentación del modelo de Bohr
En el modelo de Bohr semi-clásico, el electrón gira alrededor del núcleo en una órbita circular, como un planeta entorno al sol. Un electrón en órbita alrededor de un núcleo tendría que irradiar perdiendo energía bajo la forma de radiación y terminaría por caer en el núcleo. Este fenómeno no se produce porque los átomos son estables. Bohr supuso que existían ciertas órbitas en las cuales el electrón no emite radiación. Esta condición es válida cada vez que el momento de cantidad de movimiento del electrón es múltiplo entero de h/2π (donde h es la constante de Planck
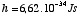
): se notan 1,2,...,n las órbitas sucesivas permitidas.
Aplicación al átomo de hidrógeno
Se considera el átomo de hidrógeno. Su electrón solo se puede encontrar en una de esas órbitas. Cada órbita corresponde a un estado de energía del átomo : el nivel de energía más bajo, el nivel fundamental notado n=1, corresponde a la órbita más próxima del núcleo. Cuanto más grande sea n, mayor será el radio de la órbita, y mayor será la energía del átomo. El valor de n infinito corresponde a una órbita de radio infinito, o sea a la ionización del átomo. La energía correspondiente es de 13,6eV.
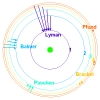
El átomo de hidrógeno sólo puede emitir o absorber fotones con una energía bien definida.
Cuando un electrón cae de un nivel excitado a un nivel de menor energía, hay una emisión de radiación que transporta exactamente la energía correspondiente a la diferencia de energía de los dos niveles.
Para que haya emisión es necesario que la energía del nivel inicial sea mayor a la del nivel final, es decir E
n > E
m, n siendo el nivel inicial y m el nivel final. La física cuántica demuestra que para el átomo de hidrógeno, la energía de los diferentes niveles de energía están definidos por la expresión siguiente :
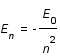
donde n entero está definido como la diferencia de niveles, E
o es la energía necesario para ionizar el átomo de hidrógeno desde du estado fundamental (su valor es 13,6eV).
El fotón emitido tiene una energía igual a la diferencia de energía entre las dos órbitas, o sea E
m-E
n. Esta energía corresponde, según la ecuación de Planck, (E=hν), a una onda electromagnética de frecuencia ν. El salto de energía se manifiesta por una línea de emisión en el espectro del átomo. Se deduce por lo tanto :
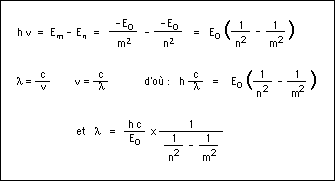
o
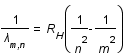
con la constante de Rydberg :
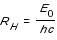
El átomo de hidrógeno también puede absorber energía que le permite de pasar de un nivel inferior de energía a un nivel superior, por ejemplo absorbiendo un fotón. Pero este fenómeno es solamente posible si el fotón posee exactamente la energía necesaria, es decir la diferencia de energía entre el nivel final y inicial.

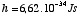 ): se notan 1,2,...,n las órbitas sucesivas permitidas.
): se notan 1,2,...,n las órbitas sucesivas permitidas.