
 Les états quantiques de l'hydrogène et de l'oxygène
Les états quantiques de l'hydrogène et de l'oxygène
Exercice d'évaluation
Difficulté : ☆☆
Le principe de Pauli interdit aux électrons d'avoir les mêmes nombres quantiques (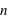 ,
, 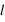 ,
, 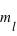 et
et 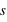 ) dans un atome. L'atome d'hydrogène 1H confine un électron sur une couche électronique (
) dans un atome. L'atome d'hydrogène 1H confine un électron sur une couche électronique (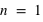 ) autour de son noyau, et l'atome d'oxygène 8O confine huit électrons répartis sur deux couches électroniques (
) autour de son noyau, et l'atome d'oxygène 8O confine huit électrons répartis sur deux couches électroniques (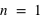 et
et 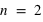 ) autour de son noyau.
) autour de son noyau.
Question 1)
Un électron peut-il être ajouté sur la couche électronique (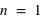 ) de l'atome d'hydrogène ?
) de l'atome d'hydrogène ?
AideSolution
Oui, d'après le Principe de Pauli, deux électrons peuvent appartenir à une même couche électronique (ou orbite atomique) s'ils ont un spin différent. Pour n=1, on a comme états quantiques possibles : l=0, ml=0, s=1/2 et l=0, ml=0, s=-1/2. L'atome devient l'ion (ou anion) 1H-.
Question 2)
Combien d'électrons peuvent-ils être ajoutés à l'atome d'oxygène ? Quels ions en découlent-il ?
Solution
La première couche contient deux électrons de spin différent, chacun ayant un état quantique différent (n=1, l=0, ml=0, s=1/2 et -1/2). La deuxième couche contient les états quantiques suivants (n=2, l=0, ml=0, s=1/2 et -1/2) et (n=2, l=1, ml=-1, s=1/2 et -1/2), (n=2, l=1, ml=0, s=1/2 et -1/2) et (n=2, l=1, ml=1, s=1/2 et -1/2), soit 4 cases quantiques pour 8 états quantiques. L'atome d'oxygène est un système à 10 états quantiques pour 8 électrons, donc deux états restent libres pour y ajouter un ou deux électrons. L'atome devient alors l'ion 8O- (ion peroxyde) ou 8O2- (ion oxyde).
Question 3)
Plutôt que de leur ajouter des électrons, ces atomes peuvent partager des électrons (électrons de valence) tout en respectant le principe de Pauli. Quelles molécules peuvent-elles être crées avec deux atomes H et deux atomes O ?
Solution
Une molécule a une valence nulle. Nous avons vu que l'hydrogène n'a qu'un état quantique de libre à partager, et l'oxygène deux. On peut donc former les molécules de dihydrogène H2 (H-H, 1 électron de valence pour chaque H), de dioxygène O2 (O=O, 2 électrons de valence pour chaque O), d'eau H2O (H-O-H, 1 électron de valence pour chaque H et 2 électrons de valence pour O), de peroxyde d'hydrogène H2O2 (H-O-O-H, 1 électron de valence pour chaque H et 2 électrons de valence pour chaque O). L'assemblage OH n'est pas une molécule, mais un radical (hydroxyde) car il reste un état quantique de libre (une valence). Le radical -OH est présent dans les molécules d'alcool (méthanol, ethanol, butanol, etc.)
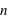 ,
, 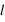 ,
, 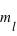 et
et 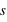 ) dans un atome. L'atome d'hydrogène 1H confine un électron sur une couche électronique (
) dans un atome. L'atome d'hydrogène 1H confine un électron sur une couche électronique (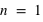 ) autour de son noyau, et l'atome d'oxygène 8O confine huit électrons répartis sur deux couches électroniques (
) autour de son noyau, et l'atome d'oxygène 8O confine huit électrons répartis sur deux couches électroniques (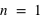 et
et 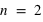 ) autour de son noyau.
) autour de son noyau.
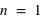 ) de l'atome d'hydrogène ?
) de l'atome d'hydrogène ?