
|
Avant d'en venir à la nucléosynthèse primordiale, un rapide bilan des connaissances sur les atomes et leur structure est entrepris.
Le terme atome a été utilisé, au XIXe siècle, pour désigner des particules qui ne peuvent se casser, du grec a-tomos. A cette époque, on croyait avoir découvert les briques élémentaires de la physique, classées dans le célèbre tableau de Mendeleïev. Le XXe siècle a cassé cette vision. Les atomes sont en vérité constitués de protons, de neutrons et d'électrons.
Un atome est composé de trois types d'éléments, neutrons, protons et électrons. Les neutrons et protons sont unis par la force nucléaire forte au sein d'un noyau d'une taille de l'ordre du femtomètre (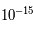 m). Les électrons sont liés par la force électromagnétique et "orbitent" autour du noyau atomique. Le terme "orbiter" comme pour les planètes est faux mais bien commode. Pour bien appréhender l'électron, il faudrait utiliser la mécanique quantique, parler d'onde de probabilité et de quantification de l'énergie, etc. Pour ce cours, on supposera que toutes les particules sont des billes très petites ; la vérité est plus complexe mais cette simplification est suffisante pour notre propos. Les électrons orbitent donc à une distance de
m). Les électrons sont liés par la force électromagnétique et "orbitent" autour du noyau atomique. Le terme "orbiter" comme pour les planètes est faux mais bien commode. Pour bien appréhender l'électron, il faudrait utiliser la mécanique quantique, parler d'onde de probabilité et de quantification de l'énergie, etc. Pour ce cours, on supposera que toutes les particules sont des billes très petites ; la vérité est plus complexe mais cette simplification est suffisante pour notre propos. Les électrons orbitent donc à une distance de 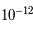 m du noyau. Les masses du proton et du neutron sont sensiblement les mêmes,
m du noyau. Les masses du proton et du neutron sont sensiblement les mêmes, 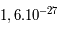 kg, alors que celle de l'électron est de l'ordre de
kg, alors que celle de l'électron est de l'ordre de 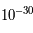 kg ; l'électron est donc 1800 fois moins massif qu'un proton. Cela entraîne qu'un atome est constitué d'un noyau très dense contenant 99.99 % de la masse autour duquel orbitent des électrons de masses négligeables. Un atome est donc principalement constitué de vide.
kg ; l'électron est donc 1800 fois moins massif qu'un proton. Cela entraîne qu'un atome est constitué d'un noyau très dense contenant 99.99 % de la masse autour duquel orbitent des électrons de masses négligeables. Un atome est donc principalement constitué de vide.
| Masse | Charge | |
| Proton | 1,672.10-27 | e |
| Neutron | 1,674.10-27 | 0 |
| Électron | 9,1.10-31 | -e |